
tanıtım
İçindeki nitrojene dikkatlice bakarsanızDI Mendeleev kimyasal elementlerin periyodik sisteminde, değişken bir valansa sahip olduğunu görebilirsiniz. Bu, azotun aynı anda oksijen ile birkaç ikili bileşik oluşturduğu anlamına gelir. Bazıları geçenlerde keşfedildi ve bazıları birlikte ve birbirlerine bakıldı. Küçük ve dengeli azot oksitler vardır. Bu maddelerin her birinin kimyasal özellikleri tamamen farklıdır, bu nedenle bunları incelemede en az beş azot oksidi düşünülmelidir. Bu onlar için ve bugünün makalesinde tartışılacak.
Nitrik oksit (I)

özellikleri
Sıradan koşullarda, renksiz bir gaz ile temsil edilir,Tatlı bir kokusu olan Su, etanol, eter ve sülfürik asidi çözebilir. Tek değerli nitrojen gazı monoksit, 40 atmosfer basınç altında oda sıcaklığına ısıtılırsa, renksiz bir sıvıya kadar kalınlaşır. Bu, ısıtma esnasında ayrışan ve reaksiyonlarda bir indirgeyici ajan olarak kendini gösteren, tuz oluşturmayan bir oksittir.
resepsiyon
Bu oksit, kuru amonyum nitrat ısıtıldığında oluşur. Bunu elde etmenin bir başka yolu, "sülfamin + nitrik asit" karışımının termal bozunmasıdır.
uygulama
Için bir araç olarak kullanılırinhalasyon anestezisi, gıda endüstrisi bu oksidi katkı maddesi E942 olarak bilir. Aynı zamanda içten yanmalı motorların performansını da geliştirir.
Nitrik oksit (II)
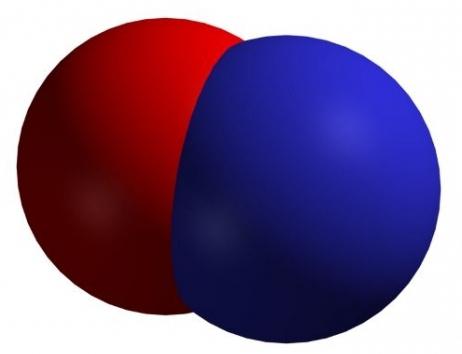
özellikleri
Normal şartlar altında renksiz bir görünüm sergiliyorgaz, suda az çözünür. Sıvılaştırmak zordur, ancak katı ve sıvı hallerde bu maddenin mavi rengi vardır. Bu oksit hava oksijeniyle oksitlenebilir
resepsiyon
Elde edilmesi oldukça kolaydır, 1200-1300 ısıtılması gerekiryaklaşıkAzot ve oksijen karışımı ile. Laboratuvarda, hemen birkaç deneyle oluşturulur:
uygulama
Nitrik asitin üretildiği maddelerden biridir.
Nitrik oksit (III)
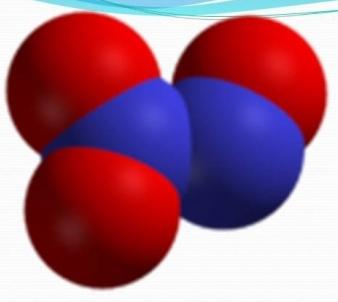
özellikleri
Normal koşullar altında, mavi bir renge ve standart şartlara sahip bir sıvıdır - renksiz bir gazdır. Saf oksit sadece katı bir agrega halinde bulunur.
resepsiyon
% 50 nitrik asit ve trivalent arsenik katı oksit etkileşimi ile oluşur (aynı zamanda nişasta ile değiştirilebilir).
uygulama
Bu madde ile, nitröz asit ve tuzları laboratuarlarda üretilmektedir.
Nitrik oksit (IV)

özellikleri
Soyadı, özelliklerinden birine karşılık gelir. Sonuçta, bu oksit ya kırmızı-kahverengi gaz ya da sarımsı bir sıvı formundadır. Yüksek kimyasal aktivite ile karakterizedir.
resepsiyon
Bu oksit, nitrik asit ve bakırın etkileşimi ve kurşun nitratın termal ayrışması sırasında elde edilir.
uygulama
Bununla birlikte sülfürik ve nitrik asitler üretilir, oksitlenmiş sıvı roket yakıtı ve harmanlanmış patlayıcılar.
Nitrik oksit (V)
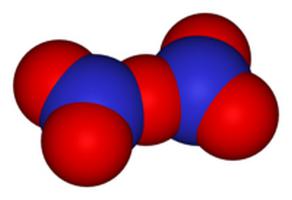
özellikleri
Renksiz ve çok uçucu kristaller formuna sahiptir. Onlar 32.3 bir sıcaklıkta eriyebiliryaklaşıkS.
resepsiyon
Bu oksit çeşitli reaksiyonlarla oluşur:
uygulama
Saf formundaki aşırı dengesizliği nedeniyle hiçbir yerde kullanılmamaktadır.
Sonuç
Kimyada dokuz azot oksit var.Yukarıdakiler bu elementin sadece klasik bileşikleridir. Kalan dördü, zaten söylendiği gibi, dengesiz maddelerdir. Bununla birlikte, hepsi bir özelliği paylaşır - yüksek toksisite. Nitrojen oksitlerin atmosferdeki emisyonları, endüstriyel kimyasal tesislerin yakınında yaşayan insanların sağlık durumlarında bir bozulmaya yol açmaktadır. Bu maddelerin herhangi biri tarafından zehirlenme belirtileri - toksik pulmoner ödem, merkezi sinir sisteminin bozulması ve kan hasarı, bunun nedeni - hemoglobinin bağlanması. Bu nedenle, nitrojen oksitlerin dikkatli kullanılması ve çoğu durumda koruyucu ekipman kullanılması gerekir.
